Ekaterinburg, Ekaterinburg, Russian Federation
Dental-Vera LLC (Acting Chief Physician, Dentist)
Ekaterinburg, Ekaterinburg, Russian Federation
Ekaterinburg, Ekaterinburg, Russian Federation
from 22.09.2014 until now
Ural State Medical University (kafedra hirurgicheskoy stomatologii i chelyustno-licevoy hirurgii, assistant)
from 01.01.2015 until now
Russian Federation
Background. A comparative study of the dynamics of iodine desorption from drugs containing iodoform and used after tooth extraction to preserve blood clots and prevention, treatment of inflammatory complications. This took into account the type and form of drugs. The content and desorption of iodine determine the duration of local exposure to the drug on the tissues of the tooth well. Objectives. To study the physico-chemical properties of iodoform containing topical preparations for the prevention and treatment of alveolitis of the jaw. Methods. The objects of the study were complex multicomponent preparations of domestic production, presented in the dental market in the form of gauze bandage, collagen sponge, paste, powder containing iodoform. A standard titrimetric method was used to quantify the iodine content in aqueous systems. For the analysis of changes of iodine content in aqueous model systems applied to the spectrophotometric method in which the concentration of a substance was assessed according to the calibration chart from 0 minutes to 48 hours. In the model solution, the albumin and pH were changed, iodine concentration was determined in 1, 15 and 30 min. Results. Medications significantly differed in both the number of iodoform and desorption in the aquatic environment of the iodine. However, the content of iodoform in the preparations did not exceed the maximum permissible concentration. Desorption of iodine from the bandage after 15 minutes is significantly less than from the viscose flagellum. Desorption of iodine from the collagen sponge remains constant for 24 hours., but increases after 48 hours. Desorption of iodine from the powder is reduced after 45 minutes. Desorption of iodine from the paste gradually increases, reaches a maximum of 105 minutes and persists after 48 hours. In the albumin-bound state, iodine is more easily desorbed in an acidic medium, and at low concentrations of iodine, desorption in a neutral medium is significantly less. Conclusions. The duration of action of iodoform when applied topically affect the dosage form of the carrier (fiber, sponge, paste, powder), the concentration of the drug, the pH and albumin content in the aqueous medium.
iodophorsoap drugs, desorption iodine, operation removing tooth, treatment inflammatory complications, alveolitis jaw
Введение
Операция по удалению зуба ― самое распространенное хирургическое вмешательство на амбулаторном стоматологическом приеме [1, 6, 22]. После проведения этапа гемостаза в зубной альвеоле образуется кровяной сгусток. Заживление раны протекает вторичным натяжением в течение 7―10 суток. Сгусток крови играет важную роль в лунке удаленного зуба для ангиогенеза и образования грануляционной ткани. Его сохранение в послеоперационном периоде является важным фактором профилактики воспалительных осложнений. В связи с этим врачами-стоматологами используются различные способы стабилизации кровяного сгустка в лунке зуба.
На заживление лунки зуба могут влиять разные факторы: наличие воспаления в тканях периодонта/пародонта до операции по удалению зуба, повреждение тканей зубочелюстного сегмента при выполнении операции, наличие соматической патологии у пациента, несоблюдение пациентом рекомендаций по уходу за полостью рта в послеоперационном периоде и т.д. [10, 13, 15, 17, 18, 21, 22]. Риск развития осложнения возрастает при травматичном удалении зуба, использовании высоких доз местного анестетика с вазоконстриктором, низком уровне гигиены полости рта.
Развитие послеоперационных воспалительных осложнений сопровождается ярко выраженным болевым синдромом, отеком тканей, появлением неприятного запаха, разрушением сгустка крови с оголением костных стенок лунки зуба. Основными задачами при лечении в таких случаях являются уменьшение боли, отека, подавление роста патогенных микроорганизмов в лунке удаленного зуба [19, 23―25].
В литературе разных лет можно найти большое количество научных работ, посвященных проблеме профилактики и лечения послеоперационных осложнений (кровотечение, альвеолит челюсти, сухая лунка) [5, 7, 16, 17, 20]. С этой целью используют различные лекарственные средства для местного применения, содержащие антисептики, антибиотики, ферменты, местные анестетики, гемостатики, гормоны, биоактивные препараты, которыми пропитывают марлевые турунды, вискозные жгутики, коллагеновые губки, пасты, гели и т.п. [2―4, 7, 9, 14, 16, 17, 20].
Лекарственные средства местного применения на основе йодоформа (растворы, порошки, пасты, губки, жгутики), оказывающие антисептическое, дезинфицирующее, бактерицидное, противогрибковое, противопротозойное и противовирусное действие, широко используются в стоматологии [7, 8]. Йод, который выделяется при гидролизе йодоформа, образует с белками клетки бактерий иодамины, коагулирует их и вызывает гибель микроорганизмов [12]. Побочным продуктом взаимодействия является муравьиная кислота, которая оказывает раздражающее действие на биологические ткани.
Сегодня на фармакологическом рынке в большом количестве представлены препараты с целью местного применения для лечения альвеолита челюсти. Однако нет достаточного количества научных данных для выбора и применения лекарственных средств, содержащих йодоформ. Необходимо проведение сравнительного исследования с целью объективной оценки эффективности различных материалов для профилактики и лечения послеоперационной боли, альвеолита челюсти.
Цель исследования ― изучить физико-химические свойства йодоформсодержащих препаратов местного применения для профилактики и лечения альвеолита челюсти.
Материалы и методы исследования
Объектами исследования стали сложносоставные многокомпонентные препараты отечественного производства, представленные на стоматологическом рынке и широко использующиеся в практике врача-стоматолога для местного применения после операции по удалению зуба. Они разделены на 3 группы: медицинские материалы на основе волокон, пористая лекарственная форма в виде губки, твердая лекарственна форма в виде порошка и пасты. Независимо от лекарственной формы препараты содержали йодоформ.
Препарат № 1. Бинт йодоформный марлевый (ОЭЗ «ВладМиВа», Россия) состоит из 100 % хлопка с тканными кромками,
Препарат № 2. «Альвостаз-жгутик» ― вискозный жгутик-тампон 1х100 см (
Препарат № 3. «Альвостаз-губка» ― коллагеновые кубики 1х1 см (ООО «НКФ Омега-Дент», Россия), пропитанные лекарственным раствором (трикальций фосфат, эвгенол, масло оливковое, йодоформ), обладает гемостатическим и антисептическим действием, рекомендован для профилактики и лечения альвеолита.
Препарат № 4. Губка «Альванес» ― лиофилизированная коллагеновая губка (ОЭЗ «ВладМиВа», Россия), в которую введены лидокаин, йодоформ, кровоостанавливающие компоненты, обладает гемостатическим, противовоспалительным и антисептическим действием, рекомендована для профилактики и лечения альвеолита, пародонтальных абцессов.
Препарат № 5. Порошок «Альванес» (ОЭЗ «ВладМиВа», Россия) содержит пищевой полисахарид, образующий с кровью гель, альгинат натрия, йодоформ (0,01 %), обладает кровоостанавливающим, антисептическим действием, рекомендован для обработки зубных лунок.
Препарат № 6. Антисептическая паста «Альванес» (ОЭЗ «ВладМиВа», Россия) содержит прополис (10 %), йодоформ (5 %), пчелиный воск, пастообразователь, обладает противовоспалительным, ранозаживляющим, обезболивающим, антимикробным действием, рекомендована для профилактики и лечения альвеолита.
Для количественного определения содержания йода в водных системах использовали стандартный титриметрический метод. Для анализа изменений содержания йода в водных модельных системах нами разработан спектрофотометрический метод, при котором концентрация вещества оценивалась по градуировочным графикам (рис. 1).
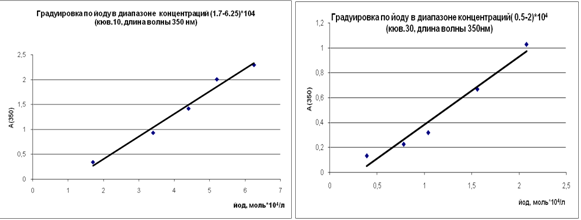
Рис. 1. Градуировочные зависимости для определения содержания йода в водных системах
Fig. 1. Calibration dependences for determination of iodine content in water systems
Для наблюдения за динамикой десорбции йода из препаратов, содержащих йодоформ, в модельный раствор (9 мл дистиллированной воды и 1 мл 0,2 % раствора альбумина) помещали такое его количество, которое в среднем возможно использовать на практике для помещения в лунку удаленного коренного зуба. Затем степень изменения концентрации йодоформа в полученных растворах оценивали спектрофотометрическим методом сразу и через каждые 15 мин. в течение 2-х часов на 1-е и 2-е сутки от начала эксперимента.
При знакомстве с инструкциями к лекарственным препаратам нами отмечено, что не все фирмы-изготовители указали количество/процентное содержание йодоформа (табл. 1).
Таблица 1
Содержание йодоформа в исследуемых препаратах
Table 1. The content of iodoform in the studied preparations
|
№ п/п |
Название препарата |
Масса, граммы |
Примечания по инструкции |
|
1. |
Йодоформный бинт (5 см) |
0,05 |
5 % йодоформ |
|
2. |
Альвостаз-жгутик ( |
0,50 |
йодоформ (кол-во не указано) |
|
3. |
Альвостаз-губка (1 шт.) |
0,07 |
йодоформ (кол-во не указано) |
|
4. |
Альванес-губка (1шт.) |
0,04 |
йодоформ (кол-во не указано) |
|
5. |
Альванес-порошок |
0,06 |
1 % йодоформ |
|
6. |
Альванес-паста |
0,57 |
5 % йодоформ |
Результаты исследования и их обсуждение
При сравнительном анализе содержания йодоформа в препаратах на основе целлюлозных волокон и хлопчатобумажных нитей нами отмечено, что в вискозном жгуте (препарат № 2) содержание йодоформа в 5 раз больше, чем в йодоформном бинте (препарат № 1), на основе коллагеновой губки: в губке «Альванес» (препарат № 4) содержание йодоформа в 2 раза больше, чем в «Альвостаз-губке» (препарат № 3), в твердых лекарственных препаратах: в порошке «Альванес» (препарат № 5) содержание йодоформа в 2,5 раза больше, чем в пасте «Альванес» (препарат № 6).
Экспериментальные данные по изменению концентрации йода в процессе десорбции йода из исследуемых препаратов в водную среду представлены в табл. 2.
Таблица 2
Изменение концентрации йода в водной среде при десорбции препаратов
Table 2. Changes in iodine concentration in the aqueous medium during desorption of drugs
|
№ препа-рата |
Концентрация йода, моль/л |
||||||||||
|
0 мин. |
15 мин. |
30 мин. |
45 мин. |
60 мин. |
75 мин. |
90 мин. |
105 мин. |
120 мин. |
24 ч. |
48 ч. |
|
|
1 |
0,8 |
0,3 |
0,4 |
0,2 |
0,2 |
0,3 |
0,3 |
0,3 |
0,2 |
0,2 |
0,4 |
|
2 |
3,9 |
3,6 |
3,5 |
3,5 |
3,4 |
3,3 |
3,5 |
3,6 |
- |
1,4 |
1,4 |
|
3 |
1,4 |
1,7 |
1,6 |
1,5 |
1,5 |
1,6 |
1,7 |
1,7 |
1,5 |
1,4 |
2,3 |
|
4 |
3,1 |
3,4 |
3,9 |
3,8 |
3,6 |
3,8 |
3,8 |
3,6 |
3,5 |
3,8 |
8,8 |
|
5 |
0,4 |
0,4 |
0,4 |
0,3 |
0,3 |
0,3 |
0,3 |
0,3 |
0,3 |
0,4 |
0,7 |
|
6 |
7,4 |
8,4 |
8,1 |
8,5 |
8,4 |
9,3 |
9,3 |
10,1 |
- |
8,4 |
10,1 |
Десорбция йода из йодоформного бинта (препарат № 1) уже через 15 минут существенно меньше, чем из вискозного жгутика (препарат № 2), из вискозного жгутика (препарат № 2) через 105 минут снижается только на 0,3 моль/л (см. табл. 2). Через 48 часов концентрация йода в водной среде из вискозного жгутика (препарат № 2) в 2,5 раза выше, чем из йодоформного бинта (препарат № 1). Исследуемые препараты отличаются физическими характеристиками волокон и содержанием йодоформа.
Марлевая турунда и вискозный жгутик относятся к волокнистым материалам, состоящим из удлиненных частиц разной длины, промежутки между которыми заполнены лекраственными веществами. Длина хлопковых волокон меньше, чем вискозных волокон, что определяет разную их толщину, упругость и сминаемость. Вискозный жгутик обладает низкой упругостью и большей сминаемостью, чем марлевая турунда. Вискозное волокно более прочное, мягкое, в 2 раза гигроскопичнее, чем хлопчатобумажное.
При погружении в воду целлюлозных волокон молекулы воды проникают между молекулярными цепями целлюлозы, раздвигают их и вызывают набухание волокна. В волокнах хлопка молекулы целлюлозы расположены более плотно, чем в вискозе, связи между ними более прочные, поэтому их набухание меньше набухания вискозных волокон. Набухание вискозы протекает медленно. Физические свойства волокон определяют характер десорбции. Необходимо отметить, что лечебный эффект марлевой турунды, пропитанной йодоформом, на 2-е сутки в 2 раза ниже, что подтверждает рекомендацию в практической стоматологии о смене турунд на 2-3-е сутки от начала лечения. В вискозном жгутике на 2-е сутки десорбции концентрация йодоформа в 2,7 раза меньше первичного значения, но в 3,5 раза выше, чем в марлевой турунде (см. табл. 2).
Десорбция йода из коллагеновой губки (препараты № 3 и 4) остается постоянной в течение 24 ч., но увеличивается через 48 ч. Препарат № 3 ― «Альвостаз-губка» ― на 2-е сутки десорбции концентрация йода увеличилась в 1,6 раза, препарат № 4 ― губка «Альванес» ― на 2-е сутки десорбции концентрация йода увеличилась в 2,8 раза. Исследуемые препараты отличаются по сорбционной характеристике на 2-е сутки, что, скорее всего, связано с технологией изготовления препарата, диффузионной проницаемостью губки, ее фильтрационной способностью, скоростью рассасывания коллагена, содержанием йодоформа в губках.
Губка имеет пористую, сетчатую структуру, внутренняя поверхность которой значительно больше, чем наружная. Пористая структура задается при синтезе и зависит от условий его проведения. Губка может поглощать жидкости, масса которых во много раз превышает ее собственную массу. Существенным недостатком коллагеновой губки является отсутствие антимикробного действия. Антимикробную активность губке придает включение в ее состав противомикробных или антисептических средств, что имеет важное значение, поскольку раны регенерируют в условиях возможного инфицирования.
Десорбция йода из порошка (препарат № 5) снижается через 45 мин. на 0,1 моль/л, а через 24 ч. увеличивается на 0,3 моль/л (см. табл. 2).
Свойства порошка при свободной насыпке определяются плотностью материала, размером и состоянием поверхности частиц, способностью сцепления между ними. Большая удельная поверхность порошка способствует активному поглощению воды, что значительно сокращает местный лечебный эффект таких лекарственных веществ в полости рта, где присутствует большое количество ротовой жидкости.
Десорбция йода из пасты (препарат № 6) постепенно увеличивается, достигает максимума через 105 мин. и концентрация йода сохраняется через 48 ч. (см. табл. 2).
Твердая лекарственная форма в виде пасты обладает большой вязкостью, упругостью, пластичностью, невысокой механической прочностью, может набухать. В связи с агрегатной устойчивостью десорбция йода из пасты происходит очень медленно. Изменение вязкости пасты, ее набухание при нахождении во влажной среде повышает десорбцию. Однако разрушение пространственных структур в пасте ― достаточно сложный процесс, поэтому характер десорбции пасты длительное время может быть на одном уровне.
Согласно инструкции фирмы-изготовителя, препараты № 5 (порошок) и 6 (паста) содержат 1 и 5 % йодоформа соответственно. Если предположить, что количество йодоформа одинаковое в составе этих препаратов, то можно заключить, что на десорбцию йода из препаратов твердой лекарственной формы влияют компоненты их состава.
Допустимая концентрация поступления йода в организм ― 2000 мкг в сутки. Из полученных экспериментальных данных не сложно рассчитать, что даже при самой высокой концентрации йодоформа в исследуемых препарататах поступление йода в организм не превысит 900 мкг в сутки.
Таким образом, лекарственные препараты существенно отличаются как по количеству йодоформа, так и по десорбции в водную среду йода ― основного противомикробного, антисептического агента. Поскольку йод может удерживаться альбумином и десорбция зависит от рН среды, то были выполнены эксперименты с модельными растворами для анализа влияния вышеперечисленных факторов. В модельном растворе изменялось содержание альбумина, рН для определения концентрации йода через 1, 15 и 30 мин. (рис. 2, 3).
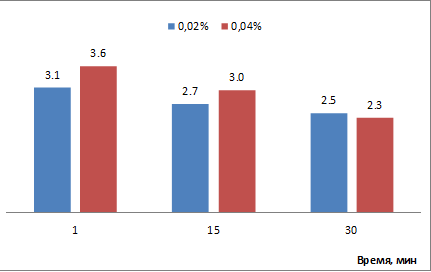
Рис. 2. Изменение концентрации йода (моль*106/л) в модельном растворе при 0,02 и 0,04 % содержании альбумина в течение 30 минут
Fig. 2. Change in iodine concentration (mol*106/l) in the model solution at 0,02 and 0,04 % albumin content for 30 minutes
Концентрация йода через 1 и 15 мин. в растворе с 0,04 % содержанием альбумина на 0,3-0,5 единицы выше, чем в растворе с 0,02 % содержанием альбумина (см. рис. 2). Через 30 мин. концентрация йода в растворах с разным содержанием альбумина почти одинаковая. Следовательно, увеличение содержания альбумина в водной среде с 0,02 до 0,04 % существенно не влияет на адсорбцию йода.
Концентрация йода в модельных водных растворах с разным рН при 0,02 % содержании альбумина представлена на рис. 3. Йод из связанного с альбумином состояния десорбируется легче в кислой среде. При низкой концентрации йода десорбция при рН ≥5,5 существенно меньше. Безусловно, это связано с конформацией альбумина при указанных значениях рН.
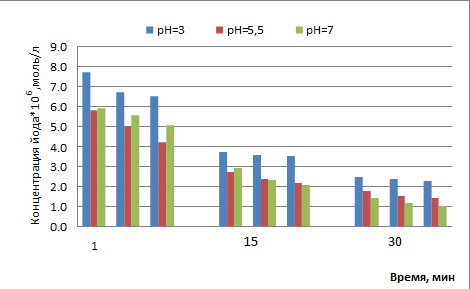
Рис. 3. Изменение концентрации йода (моль*106/л) при 0,02 % содержании альбумина в модельных растворах с рН = 3,0; 5,5, и 7,0 в течение 30 минут
Fig. 2. Change in iodine concentration (mol*106/l) at 0,02 % albumin content in model solutions with pH = 3,0; 5,5 and 7,0 for 30 minutes
Использование местного лечения лунки широко описано в литературе, хотя отмечено, что перевязочные материалы задерживают заживление лунки удаленного зуба. Различные лекарства и системы носителей доступны для использования, но иногда не имеют научных доказательств эффективности. На фармакологическом рынке регулярно появляются новые препараты для лечения одонтогенных воспалительных заболеваний, однако каждый из них имеет преимущества и недостатки. Не все предложенные препараты для местного лечения и профилактики альвеолита челюсти нашли применение в практической стоматологии, они не всегда обеспечивают длительное воздействие на ткани воспаленной лунки зуба, так как быстро вымываются слюной или самостоятельно удаляются из лунки зуба при приеме пищи, разговоре или любой другой двигательной активности жевательных мышц [9].
По данным литературы последних лет, все большее предпочтение отдается препаратам на основе коллагена, которые удобны в обращении, оказывают лечебный и профилактический эффекты, поглощают образующийся экссудат в лунке, предупреждают его скопление под раневым покрытием, легко вводятся в лунку и не требуют удаления, так как способны к рассасыванию. Выбор метода лечения и профилактики альвеолита челюсти остается спорным вопросом, так как ни один описанный в литературе метод не получил всеобщего признания [11].
Выводы
Концентрация йодоформа в исследуемых препаратах отличалась в 2; 2,5 и 5 раз, но содержание йода, который выделяется в процессе гидролиза йодоформа, не превышает предельно допустимой концентрации поступления данного микроэлемента в сутки в организм человека. Однако содержание йодоформа в препаратах должно быть ограничено ввиду того, что конечным продуктом гидролиза йодоформа является муравьиная кислота, которая будет оказывать раздражающее действие на ткани пародонта, особенно при наличии гнойного отделяемого или рН=6 в лунке удаленного зуба.
Пролонгированность действия йодоформа зависит от лекарственной формы препарата: десорбция йода из марлевой турунды происходит в 1,6 раза быстрее, чем из порошка, в 3,5 раза быстрее, чем из вискозного жгутика, в 5,7 раза быстрее, чем из коллагеновой губки и в 25,2 раза быстрее, чем из пасты.
В связанном с альбумином состоянии йод десорбируется легче в кислой среде, а при низкой концентрации йода десорбция в нейтральной среде существенно меньше.
Степень и пролонгированность выхода йодоформа из препаратов разной лекарственной формы (марлевый бинт, вискозный жгутик, коллагеновая губка, паста) необходимо учитывать врачу-стоматологу при лечении и профилактике альвеолита челюсти, так как их использование не одинаково при оценке послеоперационной боли, отека в лунке удаленного зуба, сроков заживления лунки, кратности послеоперационных посещений пациентом для выполнения осмотра, перевязок.
1. Badalyan, L. A., Shirkova, T. A., Kostina, I. N. (2017). Sovremennaya ekzodontiya_ retrospektivnoe issledovanie prichin udaleniya zubov [Modern endodontics: a retrospective study of the causes of tooth extraction]. Materiali 2 Mejdunarodnoi nauchno-prakticheskoi konferencii molodih uchenih i studentov [Materials of the 2 International scientific-practical conference of young scientists and students], 3, 33-37. (In Russ.)
2. Verlockii, A. E. (1960). Hirurgicheskaya stomatologiya: prakticheskoe rukovodstvo [Surgical dentistry: a practical guide]. Moscow, 343. (In Russ.)
3. Kolomiec, L. I. (1981). Effektivnost ektericida_ dimetilsulfoksida i oksacillina pri lechenii ostrih odontogennih vospalitelnih zabolevanii chelyustei [The effectiveness of the preparation of cough, DMSO and oxacillin in the treatment of acute odontogenic inflammatory diseases of the jaws]. Stomatologiya [The Dentistry]. 4, 33-35. (In Russ.)
4. Sirak, S. V. et al. (2010). Lechenie i profilaktika vospalitelno_atroficheskih oslojnenii posle udaleniya zubov [Treatment and prevention of inflammatory and atrophic complications after tooth extraction]. Vestnik Smolenskoi medicinskoi akademii [Bulletin of Smolensk medical Academy], 2, 138-139. (In Russ.)
5. Rodionov, N. T. et al. (2010). Profilaktika i lechenie alveolita [Prevention and treatment of alveolitis]. Vestnik Smolenskoi medicinskoi akademii [Bulletin of Smolensk medical Academy], 2, 10-14. (In Russ.)
6. Kostina, I. N. et al. (2018). Retrospektiva strukturi odontogennih vospalitelnih zabolevanii na ambulatornom hirurgicheskom stomatologicheskom prieme v krupnom promishlennom centre [Retrospective of the structure of odontogenic inflammatory diseases at an outpatient surgical dental reception in a large industrial center]. Problemi stomatologi [Actual problems in dentistry], 2, 78-85. (In Russ.)
7. Sirak, S. V., Sletov, A. A., Kardanova, K. H. (2011). Lechenie alveolita s ispolzovaniem antibakterialnih i gemostaticheskih sredstv [Treatment of alveolitis using antibacterial and hemostatic agents]. Medicinskii vestnik Severnogo Kavkaza [Medical Bulletin North Caucasus], 2, 42-43. (In Russ.)
8. Iordanishvili, A.,K. et al. (2017). Sravnitelnaya ocenka effektivnosti sredstv dlya lecheniya alveolita [Comparative evaluation of the effectiveness of funds for the treatment of alveolitis]. Institut stomatologii [Institute dentistry], 1, 1-3. (In Russ.)
9. Timofeev, A. A. (2007). Osnovi chelyustno_licevoi hirurgii: uchebnoe posobie [Fundamentals of oral and maxillofacial surgery: textbook]. Moscow : Med. inform. agentstvo, 696. (In Russ.)
10. Abu Younis, M. H., Abu Hantash, R. O. (2011). Dry socket: frequency, clinical picture, and risk factors in a palestinian dental teaching center. Open Dent J, 7, 5, 7-12.
11. Antonia, K. (2010). Alveolar osteitis: a comprehensive review of concepts and controversies. Int J Dent, 1, 10.
12. Arakeri, G.. Brennan, P. A. (2011). Povidone-iodine: an anti-oedematous agent? Int J Oral Maxillofac Surg, 40, 2, 173-176.
13. Blondeau, F., Daniel, N. G. (2007). Extraction of impacted mandibular third molars: postoperative complications and their risk factors. J Can Dent Assoc, 73, 325.
14. Bloomer, C. R. (2000). Alveolar osteitis prevention by immediate placement of medicated packing. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 90, 282-284.
15. Bui, C. H., Seldin, E. B., Dodson, T. B. (2003). Types, frequencies, and risk factors for complications after third molar extraction. J Oral Maxillofac Surg, 6, 1379-1389.
16. Sayed, F. et al. (2015). Comparision between Neocone, Alvogyl and zinc oxide eugenol packing for the treatment of dry socket: a double blind randomised control trial. J Maxillofac Oral Surg, 14, 2, 312-320.
17. Cho, H. et al. (2015). Complication rates in patients using absorbable collagen sponges in third molar extraction sockets: A retrospective study. J Korean Assoc Oral Maxillofac Surg, 41, 26-29.
18. Eshghpour, M., Nejat, A. H. (2013). Dry socket following surgical removal of impacted third molars in an Iranian population: Incidence and risk factors. Niger J Clin .Pract, 16, 496-500.
19. Haraji, A., Rakhshan, V. (2015). Clorhexidine gel and less difficult surgeries might reduce post-operative pain, controlling for dry socket infection and analgesic consumption: A split-mouth controlled randomised clinical trial. J Oral Rehabil, 42, 209-219.
20. Jesudasan, J. S., Wahab, P. U., Sekhar, M. R. (2015). Effectiveness of 0.2% clorhexidine gel and an eugenol-based p3ste on postoperative alveolar osteítis in patients having third molars extracted: A randomised controlled clinical trial. Br J Oral Maxillofac Surg, 53, 826-830.
21. Malkawi, Z., Al-Omiri, M. K., Khraisat, A. (2011). Risk indicators of postoperative complications following surgical extraction of lower third molars. Med Princ Pract, 20, 321-325.
22. Osborn, T. P., Frederickson, G. Jr., Small, I. A., Torgerson, T. S. (1985). A prospective study of complications related to mandibular third molar surgery. J Oral Maxillofac Surg, 43, 767-769.
23. De Santana-Santos, T. et al. (2013). Prediction of post-operative facial swelling, pain and trismus following third molar surgery based on preoperative variables. Med Oral Patol Oral Cir Bucal, 18, 65-70.
24. Rakhshan, V. (2015). Common risk factors for postoperative pain following the extraction of wisdom teeth. J Korean Assoc Oral Maxillofac Surg, 41, 2, 59-65.
25. Lago-Méndez, L. et al. (2007). Relationships between surgical difficulty and postoperative pain in lower third molar extractions. J Oral Maxillofac Surg, 65, 979-983.